三代EGFR-TKI甲磺酸伏美替尼获NMPA批准上市!
发布时间:2021-03-16作者:近日,国家药监局(NMPA)批准艾力斯医药第三代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)甲磺酸伏美替尼上市,用于治疗EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)。
我国NSCLC患者EGFR敏感突变率约为50%,这类患者常规使用第一/二代EGFR-TKI治疗,但多数患者在接受治疗一年左右出现耐药和疾病进展,其中,约60%的患者为EGFR T790M耐药突变,这类患者目前最有效的治疗药物为第三代EGFR-TKI。
一项代号为ALSC003的IIb期多中心单臂研究评估了伏美替尼治疗T790M突变NSCLC患者的疗效和安全性。研究纳入了局部晚期或转移性经一/二代EGFR TKI治疗后进展或初治T790M突变NSCLC患者,接受伏美替尼(80mg,每日1次)治疗,主要研究终点为ORR,次要终点包括DCR、PFS和OS。
临床结果
2018年6月至2018年12月期间,共纳入220例患者,其中212例患者为IV期,截止到2019年4月12日,患者ORR为73.6%(ASCO2020数据显示,ORR为74.1%),预估6周和12周DCR率为87.3%和82.3%,中位PFS为7.6个月,中位OS和DoR均未达到。
安全性方面,209名患者(95.0%)有至少一种不良事件(AE)发生,大部分为1-2级且耐受性良好。常见不良反应包括转氨酶升高、上呼吸道感染、咳嗽(发生率均在15%左右)。腹泻的发生率较低(6.0%),≥3级的腹泻为0.4%。19.1%的患者发生了3-5级AE,最常见的是γ-谷氨酰转移酶升高(n=4)。
截至目前,国内已有3款第3代EGFR-TKI上市,此前,阿斯利康的奥希替尼于2017年3月22日获NMPA批准上市,并在2018年纳入乙类医保;阿美替尼是豪森药业开发的一款三代EGFR-TKI药物,在2019年4月申报上市,被纳入优先审评,2020年3月获得NMPA批准上市,适用于既往经表皮因子受体抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性NSCLC成人患者。该药物于2020年12月被纳入新版医保。
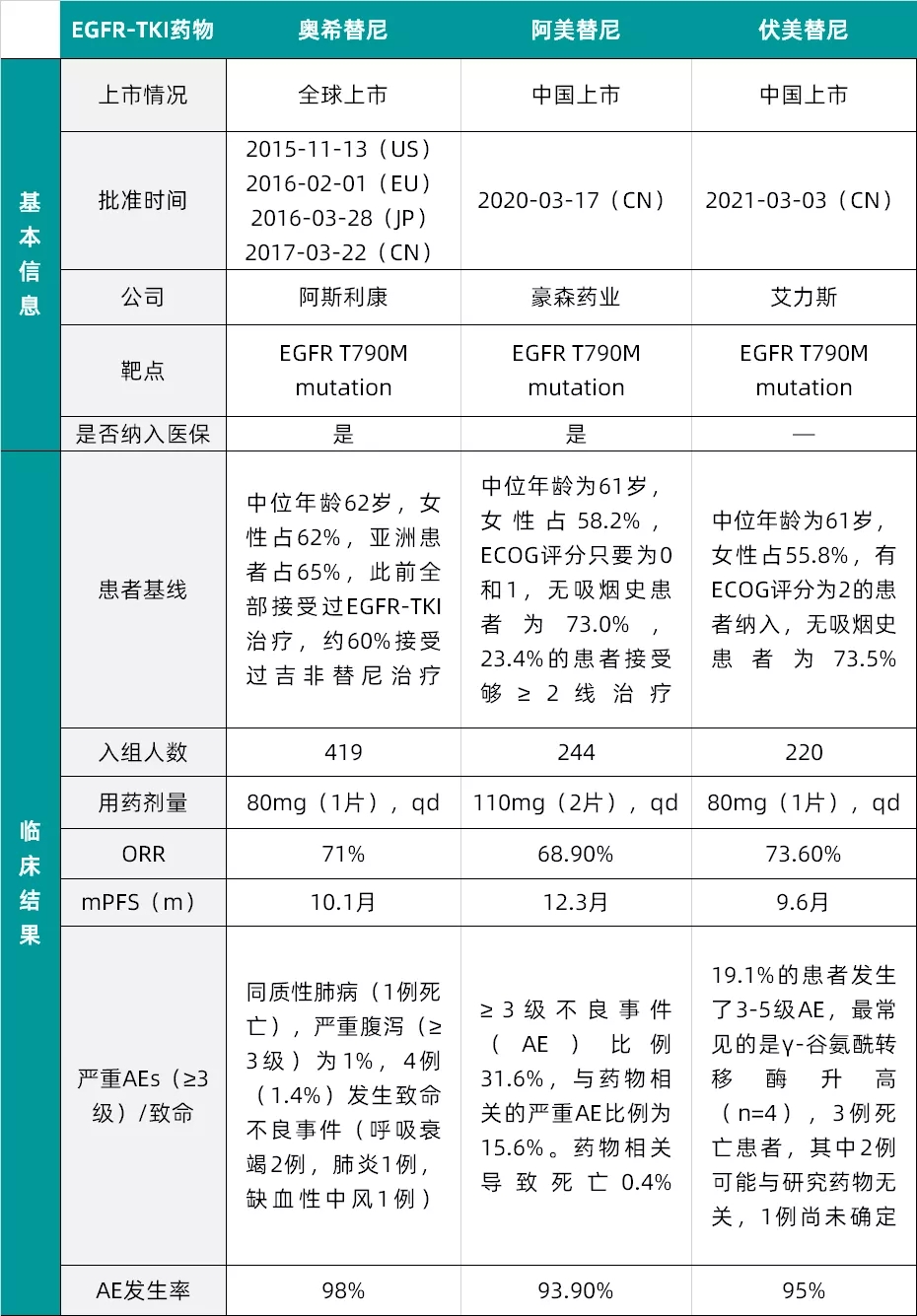
奥希替尼 vs 阿美替尼 vs 伏美替尼
>






















