奥希替尼再获新适应症:FDA批准首个NSCLC术后辅助靶向疗法
发布时间:2020-12-28作者:尽管大多数被确诊为非小细胞肺癌(NSCLC)的患者已无法采取手术切除治疗,但仍有30%的患者有望通过手术切除进行治疗。术后辅助化疗是IB~III期NSCLC的标准治疗方法,但患者5年生存率较差(约50%)。直至近期,EGFR-TKIs吹响了早期NSCLC辅助靶向治疗的号角!
2020年11月25日,NCCN NSCLC 2021.V1版指南发布,首次将奥希替尼推荐用于IB~IIIA期术后携带EGFR突变NSCLC患者的辅助治疗。同时,推荐IB~IIIA期NSCLC患者术后手术组织/活检样本应进行EGFR基因检测。1

2020年12月18日,FDA正式批准奥希替尼用于术后经FDA批准产品检测携带EGFR 19外显子缺失(19dels)及21外显子L858R突变NSCLC患者的辅助疗法(Adjuvant Therapy)。这也是FDA批准的首个NSCLC术后辅助靶向疗法!2,3

此次FDA批准是基于一项随机、双盲、安慰剂对照试验ADAURA的III期临床试验结果。
该试验总共纳入682例已完全切除肿瘤的早期非小细胞肺癌患者(非鳞癌,IB~IIIA期),这些患者经FDA批准的基因检测产品检测携带有EGFR 19外显子缺失(19dels)及21外显子L858R突变,被随机(1:1)分配接受口服奥希替尼80mg/天(339例)或安慰剂(343例,既往应用或未应用辅助化疗)进行治疗。
此次试验中使用的FDA批准检测产品为:cobas® EGFR Mutation Test,其中55%患者为19dels突变,45%患者为L858R突变。
主要疗效指标是研究者评估II–IIIA期NSCLC患者的无病生存期(DFS)。
结果显示,与安慰剂相比,奥希替尼成功延长了II-IIIA期可手术患者的中位DFS,为 未达到 (38.8,NE)vs 19.6个月(16.6,24.5),降低了83%的疾病复发或死亡风险(HR=0.17),达到主要研究终点。在研究总人群中(IB-IIIA期),奥希替尼的中位DFS同样优于安慰剂,为 未达到(NE,NE) vs 27.5个月(22,36),降低了80%的疾病复发或死亡风险(HR=0.20)。OS数据目前尚不成熟,仅有5%成熟度。
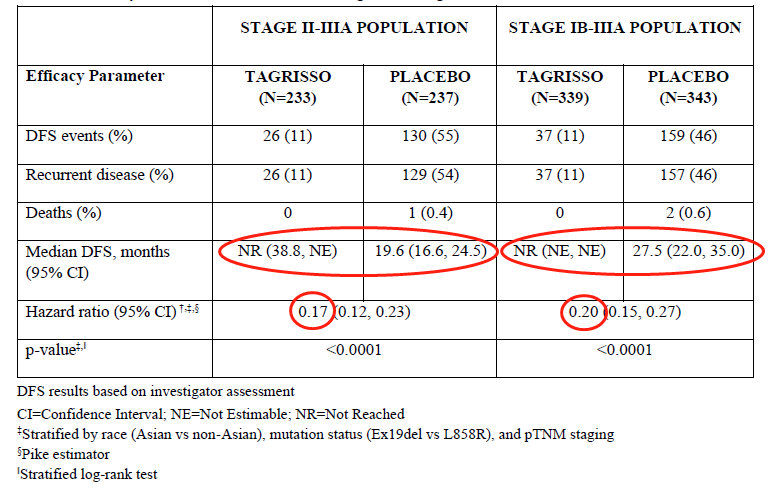
▲ ADAURA研究疗效数据
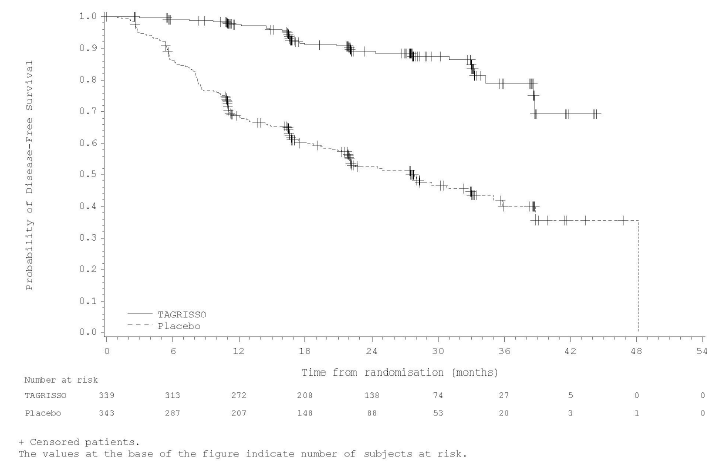
▲ ADAURA研究DFS生存曲线
奥希替尼辅助治疗最常见的副作用包括腹泻、皮疹、肌肉骨骼疼痛、皮肤干燥、指甲周围皮肤发炎、口腔疼痛、疲劳和咳嗽。如果患者出现间质性肺病症状,应停用奥希替尼,如果证实为间质性肺病,应永久停用。
如果给孕妇服用奥希替尼,可能会对胎儿造成伤害,因此,在开始奥希替尼治疗前,应确认有生育潜力女性的怀孕状况。如怀疑为Stevens-Johnson综合征或多形红斑,应停用奥希替尼。
对中国NSCLC患者的影响
在亚洲,肺癌的发病率正在上升,并且占全世界新诊断肺癌病例的一半以上,其中NSCLC约占85%。在亚洲NSCLC患者中,EGFR突变频率高达46.7%,尤其是腺癌(54.1%)和女性(61.8%)患者。
此次ADAURA研究入组的682例NSCLC患者中,64%为亚洲人,对中国NSCLC患者来说意义重大。

▲ ADAURA研究中,64%为亚洲人
2020年10月12日,中国CDE官网显示,甲磺酸奥希替尼片已被纳入优先审评,用于具有表皮生长因子受体(EGFR)敏感突变的非小细胞肺癌(NSCLC)成人患者肿瘤切除术后的辅助治疗。相信在不久的将来,中国的NSCLC患者将会获益于奥希替尼的辅助治疗,提高生存的质量。
划重点:
① EGFR-TKI(奥希替尼)已推荐用于早期(IB~IIIA期)术后携带EGFR突变NSCLC患者的辅助治疗;
② 术后辅助使用EGFR-TKI(奥希替尼,80mg/天)应至少持续2年/3年或更长时间以降低复发风险;
③ 早期NSCLC患者术后(手术组织/活检组织)应进行EGFR基因检测,有条件的患者,可以使用NGS对除EGFR以外的驱动基因进行检测(对术后复发/转移有进一步指导意义);
④ 有条件的患者,可以使用cfDNA液体活检技术识别术后NSCLC患者的最小残留病灶(MRD),进行动态监测并指导治疗。
参考资料:
1.NCCN NSCLC 2021.V1指南
2.https://www.fda.gov/news-events/press-announcements/fda-approves-first-adjuvant-therapy-most-common-type-lung-cancer
3.https://www.fda.gov/drugs/drug-approvals-and-databases/fda-approves-osimertinib-adjuvant-therapy-non-small-cell-lung-cancer-egfr-mutations
文章来源:基因talks
本文旨在传递肿瘤医药最新讯息,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。























