新靶点崛起!FGFR两款新药获批,再掀起跨癌种治疗热潮!
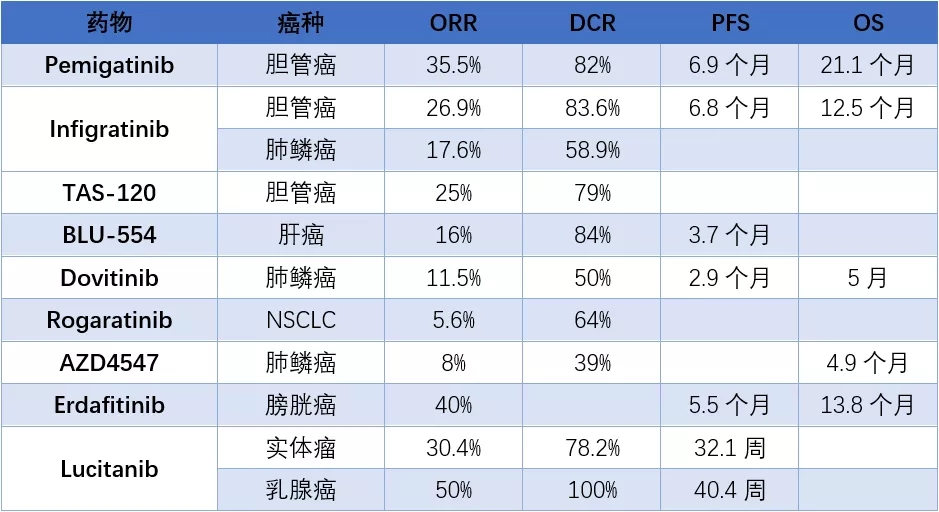
发布时间:2020-05-06作者:admin随着前几天胆管癌首个靶向药Pemigatinib的获批上市,FGFR靶点治疗逐渐崛起,这也是继去年Erdafitinib获批用于膀胱癌后的第二个FGFR抑制剂。今天就为大家介绍一类新的靶点----FGFR,中文名成纤维细胞生长因子受体。FGFR家族主要包括 FGFR1、FGFR2、FGFR3和FGFR4 4种亚型,各亚型均具有与配体结合的胞外区、跨膜区和受体磷酸化的胞内区的结构特点。是负责细胞增殖和分化的酪氨酸激酶信号通路的一部分。FGFR分子改变可导致异常的FGF/FGFR信号,促进细胞增殖、新血管生成、侵袭、转移、抗凋亡等,这与广泛的人类恶性肿瘤有关。现有药物如下。
有三种异常类型,多癌种发生的“元凶”
FGFR靶点异常可以见于各个肿瘤,在一项4853例的NGS检测结果发现,FGFR通路异常的发生频率为7%,遍布各癌种,尤其在尿路上皮癌、乳腺癌、子宫内膜癌、卵巢癌、原发灶不明等肿瘤多见。常见的FGFR通路异常包括扩增、突变和重排。其中基因扩增、基因突变以及染色体重排分别占比为66%、26%及8%;FGFR1、FGFR2、FGFR3及FGFR4在发病患者中占比为3.5%、1.5%、2.0%及0.5%。膀胱癌患者的FGFR基因异常的比例最高,为32%,乳腺癌为18%,子宫内膜癌13%,肺鳞癌13%,卵巢癌9%。具体如下:
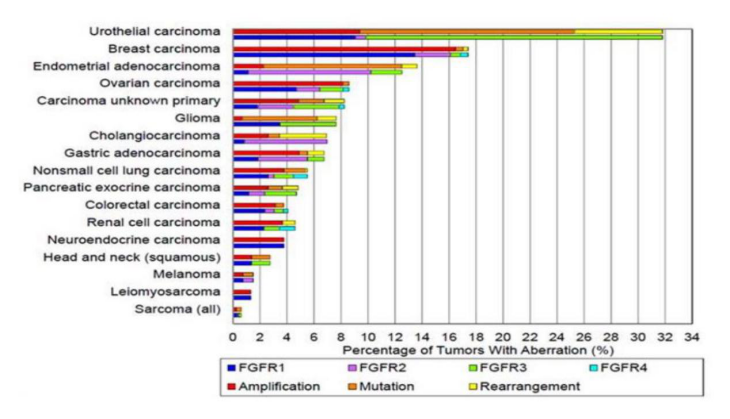
在临床上,FGFR突变可以致癌,相关的例子有:
⑴ FGFR1扩增与鳞状非小细胞肺癌、乳腺癌有关;
⑵ FGFR2突变与子宫内膜癌、胃癌有关;
⑶ FGFR2融合与肝癌有关;
⑷ FGFR3融合与骨髓瘤有关;
⑸ FGFR3突变与膀胱癌有关;
⑹ FGFR4扩增/突变已见于横纹肌肉瘤患者。
近年,多款FGFR抑制剂进入临床研究阶段,并且有2个新药获批上市,1个进入优先审评。
一.肝胆
1.Pemigatinib:近日上市,成为胆管癌首个获批靶向药
该药是针对FGFR1/2/3的强效选择性口服抑制剂,2020年4月18日获批用于治疗FGFR2基因融合或其它重排类型的经治晚期胆管癌患者。该药二线治疗晚期胆管癌患者的FIGHT202研究分为3个队列:A是FGFR2融合/重排(n=107),B是其他FGFR突变(n=20),C是非FGFR突变(n=18)。结果显示,A组ORR(客观缓解率)为35.5%,其中3例患者完全缓解(CR),CR率为2.8%,DCR(疾病控制率)为82%。B组和C组的ORR为0%。相比其他两个队列,队列A的患者对药物有效响应的比例大很多,有效时间也长得多。A组的中位DOR(缓解持续时间)为7.5个月, 中位PFS(无进展生存期)和中位OS(总生存期)分别为6.9和21.1个月。
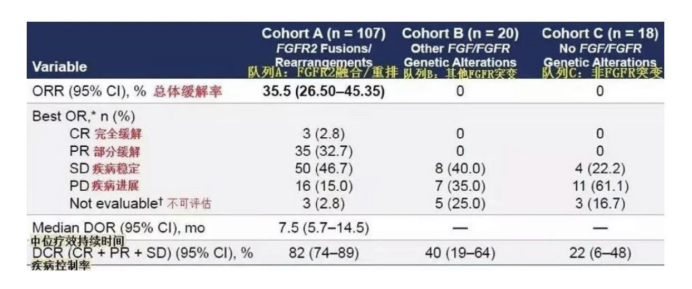
就在前不久Pemigatinib二线治疗局晚期或转移性胆管癌的Ⅱ期临床试验FIGHT-202于国际顶级期刊《柳叶刀·肿瘤学》(The Lancet Oncology)正式发表。
2.Infigratinib(BGJ398):被纳入优先审评
Infigratinib是一种口服给药的选择性FGFR-TKI,2020年1月初被FDA授予快速通道资格。既往的一项研究纳入71名患有FGFR2融合/易位的胆管癌患者,其中62%为女性患者,38%为男性患者。确认的ORR为26.9%,DCR为83.6%,中位DoR为5.4个月,中位PFS为6.8个月,中位OS为12.5个月。
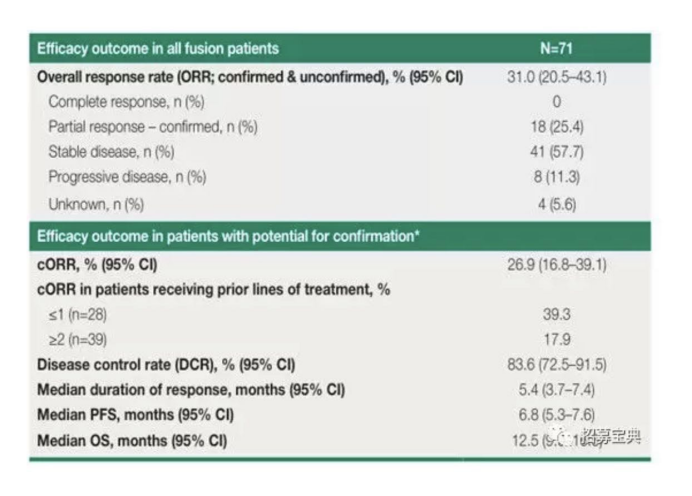
3.TAS-120:获得FDA授予孤儿药称号,可解决FGFR靶向耐药。
TAS-120为高选择性不可逆的泛FGFR抑制剂。在1期试验中,该药治疗28例FGFR2融合胆管癌患者的ORR为25%,DCR达到79%。其中4例患者对infigratinib或者其他FGFR2 抑制剂耐药,接受TAS-102治疗后,2例患者产生了部分反应,另外2例患者病情稳定,持续了5到17个月。我们期待更加成熟的数据。
基于此,FDA授予TAS-120孤儿药称号。目前该药正进行胆管癌及子宫内膜癌的剂量扩增试验。
4.肝癌:BLU-554新药后线控制率达68%
BLU-554,作用靶点是FGFR4(与FGF19配对)。I期数据初步结果显示,数据截止时共有77例患者按照RECISIST1.1(研究者评定的疗效)接受了疗效评估的患者中。在38例FGF19免疫组化阳性(IHC+)患者中,6例(16%)患者达到PR。26例(68%)患者获得SD,18例(49%)患者肿瘤负荷减小。38例FGF19IHC+患者的最大肿瘤减小(根据靶病灶缩减衡量)见图。中位PFS为3.7个月。
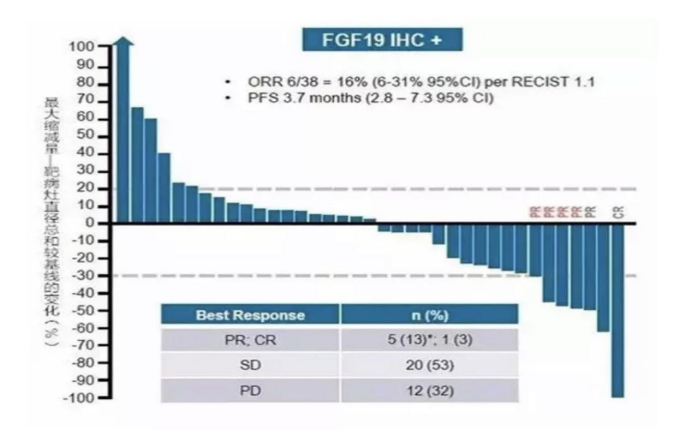
二.肺癌
在肺癌中,FGFR通路异常多见于肺鳞癌,以FGFR扩增多见。
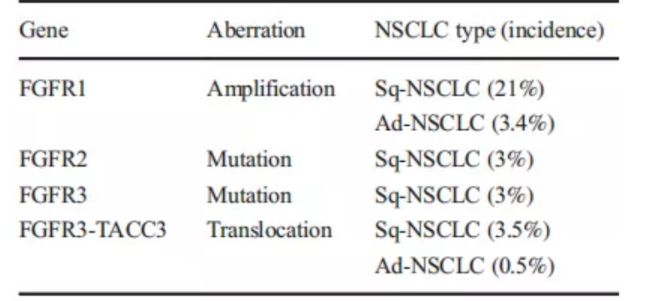
1.多韦替尼(Dovitinib)治疗FGFR1扩增肺鳞癌
该药是VEGFR/PDGFR抑制剂抑制剂。纳入人群为FGFR1扩增的晚期肺鳞癌患者。多韦替尼给药后的中位反应持续时间为2.5个月。ORR为11.5%,DCR为50%,3例患者疾病部分缓解(P R)。3例PR患者的反应持续时间分别为4.5、5.1和6.1个月。在一次15.7个月的中位随访后,中位OS为5.0个月,PFS为2.9个月。
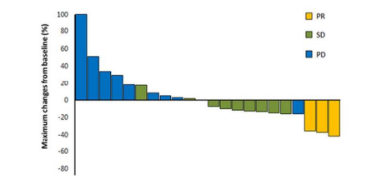
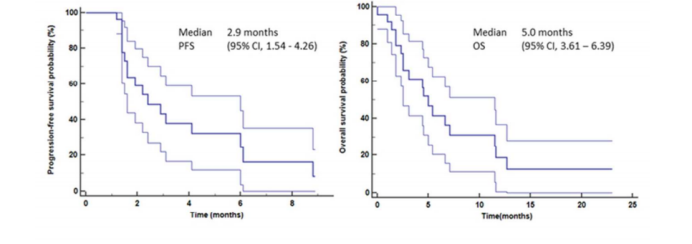
2.Rogaratinib治疗FGFR阳性NSCLC,控制率64%
该药是泛FGFR抑制剂。2019年ASCO摘要中收录了泛FGFR抑制剂rogaratinib的数据(摘要号e20661)。研究纳入了40例FGFR在mRNA中阳性的晚期NSCLC患者。ORR为5.6%(1例反应持续了16个月以上),DCR为64%。药物安全性方面,Rogaratinib的耐受性尚可,大部分为轻中度AE。
3.BGJ398治疗肺鳞癌,DCR为58.9%
BGJ398是针对FGFR1-3的小分子抑制剂。在的Ⅰ期研究,纳入了21例FGFR1扩增的肺鳞癌患者,治疗剂量为100mg/d或更高, 21名FGFR1扩增的肺鳞癌患者,17位患者疗效可评价,其中3名患者客观缓解,ORR=17.6%,7名患者疾病稳定,7名患者疾病进展;DCR为58.9%,这项佳绩也在JCO杂志上报道。

4. AZD4547治疗肺鳞癌,疾病控制率为39%
AZD4547是也一种有效的选择性FGFR1-3抑制剂,在肺鳞癌领域也有研究报道。这是一项AZD4547单药治疗肺鳞癌的Ⅰb期国际多中心试验,共有13例可评估疗效的肺鳞癌患者,所有患者均为Ⅳ期肺鳞癌,FISH检测为FGFR1扩增,所有患者均接受过一线化疗后疾病进展。
试验结果发现,13例可评估疗效的患者中,1例患者部分缓解(PR,8%),4例患者病情稳定(SD,31%),DCR为39%,中位总生存期(OS)为4.9个月。

三.膀胱
Erdafitinib上市,成为膀胱癌首个靶向药,对PD1耐药也有效
2019年4月12日,Balversa (erdafitinib)获得FDA加速批准,用于治疗铂类化疗后疾病进展的局部晚期或转移性膀胱癌成人患者,成为首个获批的转移性膀胱癌靶向疗法。
该适应症基于一项2期临床试验结果,共有87名晚期FGFR基因突变的膀胱癌患者入组。入组的患者既往都接受过至少1种方案的治疗,其中24%的患者已经接受过PD1/PDL1单抗的治疗,均告失败。结果显示,总的ORR为40%,其中有3%出现完全缓解CR。缓解者包括之前使用抗PD-L1或PD-1药物治疗无效的患者,大约四分之一的参与者之前接受过抗PD-L1/ PD-1治疗。22例PD1/PDL1耐药的患者ORR为59%。PFS为5.5个月,OS为13.8个月。
四.乳腺癌及其他实体瘤
Lucitanib治疗实体瘤(乳腺癌为主)
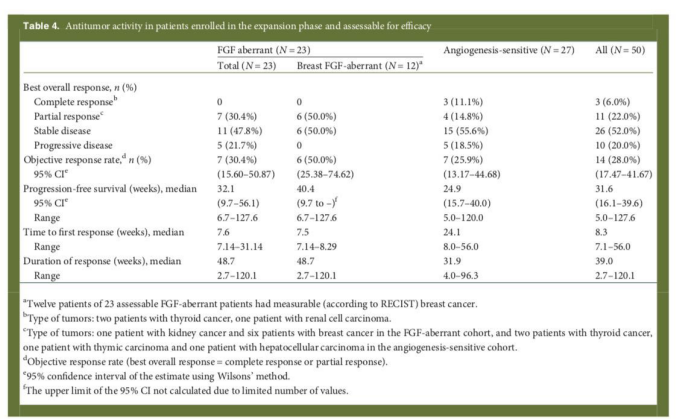
这项研究纳入人群为晚期实体瘤患者。总人群的ORR为28%,DCR为52%,中位PFS为31.6周,中位DOR为39周。FGF异常患者的ORR为30.4%,DCR为78.2%,中位PFS为32.1周,中位DOR为48.7周。在FGF异常的乳腺癌亚组中,ORR为50%,DCR为100%,中位PFS为40.4周,中位DOR为48.7周。
FGFR靶向药物的研发与临床在不断向前推进,相信未来能为癌症患者带来新的、更多的选择。FGFR靶向药,任重道远,但未来可期!
文章来源:找药宝典























